研究・開発について
従来、腫瘍治療抗体を目的として、強い反応性、結合力が想定される分子を標的として、その分子、ペプチドをマウスに免疫して抗体が樹立されてきた。しかし、その分子に対する抗体は得ることは出来ても、本当に治療効果を持った抗体を樹立することは稀で困難であった。従来の方法では抗原の立体構造は認識できないため高親和性の抗体が得られなかったことがうまくいかない原因と考えられる。
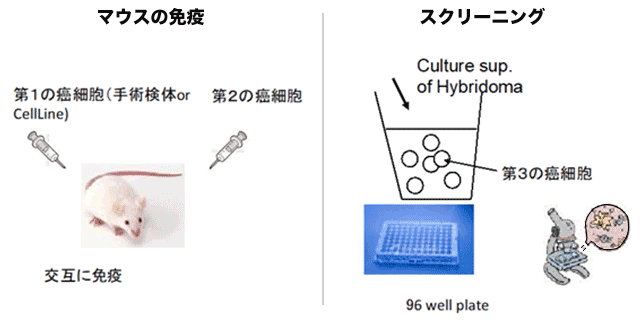
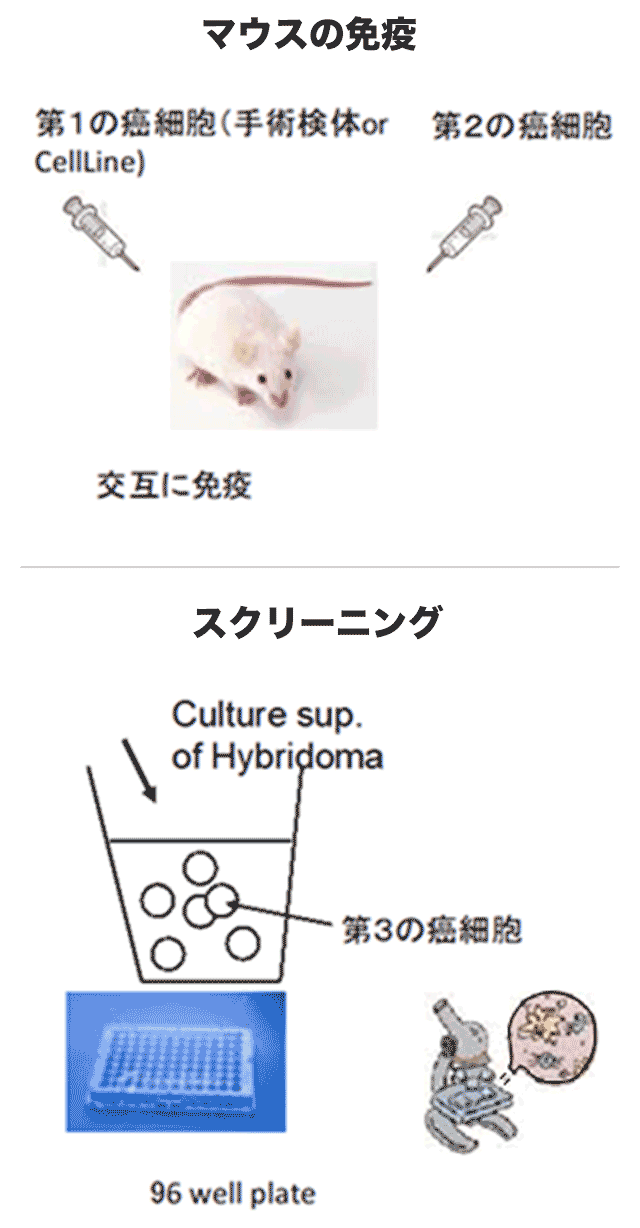
この問題点を解決する方法として、対象疾患(がん)のがん細胞(数種の細胞株を利用する方法と数人のがん患者の手術材料)を利用する方法を提案した。(Matsuoka S et al. PLoS ONE, 2016、BMC Res Notes 2016)。
何人かに由来する腫瘍組織・細胞もしくは当該癌種のcell lineを免疫して樹立した抗体は、がん細胞の表面分子の立体構造を認識可能なことに加えて、アミノ酸からなるペプチド配列だけでなく翻訳後修飾(糖鎖、リン酸化、脂質等)も含めた抗原を認識することが可能となるため、診断・治療の観点からも極めて意義のある(病態を反映した)優れた強いaffinityの抗体を樹立できる可能性が有る。さらに、生化学的な方法を用いて標的分子を確定することも可能であり、腫瘍を免疫して探索された有望抗体の抗原は今までに考えられなかった標的分子(群)、あるいは領域(エピトープ)に対する抗体である可能性も少なくないことから、新たながん治療薬を開発するために重要な創薬アプローチになると考えられる。
PLOS ONEで紹介された松岡らの抗体樹立方法にはもう一つ、ハイブリドーマ のスクリーニング方法においてもアカデミックならではの、新たな工夫がなされている。それはクローンの培養上清を96well plateに蒔かれたがん細胞に添加して、それによるがん細胞の形態学的変化を、病理学者の眼を持って観ることである。顕微鏡下に直接観ることによって、抗体の結合を判断するのである。また、このスクリーニングにおいては、免疫に用いたがん細胞にクロノティピックに反応する抗体を拾い上げる可能性を排除するため、同じがん腫で、免疫には用いなかったcell lineを標的細胞としてスクリーニングを行なうという工夫もされている。
この、複数のがん細胞のcell line を生きたまま、もしくは患者検体をそれぞれ生きた状態でマウスに免疫し、かつ抗体のスクリーニングにおいては、抗体を、そのがん腫の別のcell lineの細胞に添加し、その形態的変化を顕微鏡下に形態学的に判断するという方法は、前述したように立体構造や糖鎖を含め抗原を認識できる、affinityの高い抗体を得られるとうメリットと、今まで想定できなかった未知の抗原を認識できるという可能性を持っているという点で、今までのペプチドを免疫してFACSやELISAによってスクリーニングする方法に比べ抗体の腫瘍細胞へのダイレクトな影響を把握できるという優位性があると考えられる。
現在のペプチド免疫法に代わる我々の新しい免疫およびスクリーニング法